協和発酵バイオ「ヒトミルクオリゴ糖」新規食品に承認
執筆者:shirai
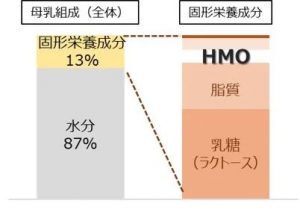 協和発酵バイオが製造・販売を行うヒトミルクオリゴ糖(Human milk oligosaccharide; 以下HMO)の2FL(2’-Fucosyllactose)が、欧州連合の欧州委員会により新規食品(Novel Food)として承認された。同承認によって、2024年8月19日より、欧州連合加盟27カ国で製造・販売する乳児用ミルクや食品に、協和発酵バイオの2FLが使用可能になる。同社が製造・販売を行うHMOについては、既に3SL(3’-sialyllactose sodium salt)、6SL(6’-sialyllactose sodium salt)が承認されている。同社は、1990年代からHMO研究開発の最前線に立ち、2000年に世界で初めて工業レベルでのHMO大量生産システムを構築。2022年11月には、タイに新設した最先端の工場でHMO 3品目(2FL・3SL・6SL)の商業生産を開始。今回の2FLの承認により、3品目が欧州にて供給可能となる。今後、新規食品原料の申請が承認された国・地域で、HMOの展開を拡大させていく。新規食品(Novel Food)とは、最初の新規食品法令が施行された1997年5月15日以前に「欧州で顕著に消費されてこなかった食品」、「新規技術を用いて製造された食品」「欧州以外の地域で伝統的に食されてきた経験のある食品」などが該当。欧州でNovel Foodを販売するためには、欧州委員会の承認を受ける必要があり、事前に欧州食品安全機関(EFSA)による科学的な安全性評価が必要に応じて実施される。同社の2FLは、2023年11月にEFSAの安全性評価で安全性が認められ※5、欧州委員会によりNovel Foodとして承認された。「ヒトミルクオリゴ糖(HMO)」とは、母乳に含まれるオリゴ糖の総称。母乳中の固形成分の中では、ラクトース、脂質に次ぐ、三番目に多い成分で、これまでに200種類以上のHMOが母乳から発見されている。牛乳や他哺乳類由来の乳にはほとんど含まれず、特にヒトの初乳に多く含まれることから、乳幼児の免疫や腸内細菌層の形成に重要な成分であることが知られている。HMO入り粉ミルク市場は欧米で継続的に伸長しているだけでなく、人口増加が見込まれる中国・東南アジア地域でも消費拡大が期待されており、今後の年平均成長率は20%~30%程度と予測されている。
協和発酵バイオが製造・販売を行うヒトミルクオリゴ糖(Human milk oligosaccharide; 以下HMO)の2FL(2’-Fucosyllactose)が、欧州連合の欧州委員会により新規食品(Novel Food)として承認された。同承認によって、2024年8月19日より、欧州連合加盟27カ国で製造・販売する乳児用ミルクや食品に、協和発酵バイオの2FLが使用可能になる。同社が製造・販売を行うHMOについては、既に3SL(3’-sialyllactose sodium salt)、6SL(6’-sialyllactose sodium salt)が承認されている。同社は、1990年代からHMO研究開発の最前線に立ち、2000年に世界で初めて工業レベルでのHMO大量生産システムを構築。2022年11月には、タイに新設した最先端の工場でHMO 3品目(2FL・3SL・6SL)の商業生産を開始。今回の2FLの承認により、3品目が欧州にて供給可能となる。今後、新規食品原料の申請が承認された国・地域で、HMOの展開を拡大させていく。新規食品(Novel Food)とは、最初の新規食品法令が施行された1997年5月15日以前に「欧州で顕著に消費されてこなかった食品」、「新規技術を用いて製造された食品」「欧州以外の地域で伝統的に食されてきた経験のある食品」などが該当。欧州でNovel Foodを販売するためには、欧州委員会の承認を受ける必要があり、事前に欧州食品安全機関(EFSA)による科学的な安全性評価が必要に応じて実施される。同社の2FLは、2023年11月にEFSAの安全性評価で安全性が認められ※5、欧州委員会によりNovel Foodとして承認された。「ヒトミルクオリゴ糖(HMO)」とは、母乳に含まれるオリゴ糖の総称。母乳中の固形成分の中では、ラクトース、脂質に次ぐ、三番目に多い成分で、これまでに200種類以上のHMOが母乳から発見されている。牛乳や他哺乳類由来の乳にはほとんど含まれず、特にヒトの初乳に多く含まれることから、乳幼児の免疫や腸内細菌層の形成に重要な成分であることが知られている。HMO入り粉ミルク市場は欧米で継続的に伸長しているだけでなく、人口増加が見込まれる中国・東南アジア地域でも消費拡大が期待されており、今後の年平均成長率は20%~30%程度と予測されている。